Problém s neplodnosťou postihuje ročne viac ako 48 miliónov párov na celom svete, čo predstavuje významnú výzvu pre modernú medicínu a vedu. Vďaka neustálemu výskumu a inováciám v oblasti asistovanej reprodukcie, konkrétne umelého oplodnenia (IVF), sa šance pre páry túžiace po dieťati neustále zvyšujú. Tento článok sa zameriava na aktuálny stav výskumu v oblasti umelého oplodnenia, výzvy, ktorým čelia vedci, a inovatívne metódy, ktoré sa vyvíjajú na zlepšenie úspešnosti IVF.
Úvod do Asistovanej Reprodukcie
Umelé oplodnenie (In Vitro Fertilization - IVF) je moderná a vysoko efektívna laboratórna technika, pri ktorej dochádza k oplodneniu vajíčka spermiou mimo maternice. V posledných rokoch sa výskum v tejto oblasti zameriava na zlepšenie všetkých aspektov procesu IVF, od výberu vhodných buniek až po kultiváciu embryí a ich implantáciu do maternice. Cieľom je zvýšiť úspešnosť IVF a minimalizovať riziká spojené s touto metódou.
Výzvy v Súčasnom Výskume Neplodnosti
Vedci sa pri riešení neplodnosti stretávajú s množstvom výziev, ktoré si mnohí ani neuvedomujú. Snahou je čo najlepšie pripraviť potenciálnu mamičku a otca, avšak vždy je kam posúvať limity. Vždy je čo zlepšovať, či prístup, či skrátiť časovú náročnosť, či spracovanie biologického materiálu a ďalšie premenné, keďže úspešnosť IVF nie je stopercentná.
Biologické Faktory
Po biologickej stránke sú to aj faktory, ktoré súvisia s výberom vhodných buniek. Napríklad pri pacientkach, u ktorých je zvýšená pravdepodobnosť onkologického ochorenia, je výzvou zabezpečiť uchovanie buniek, ktoré by jej mohli v prípade vážneho ochorenia umožniť mať dieťa. U mužov je výzvou napr. fragmentovaná DNA v mužských pohlavných bunkách. Na odseparovanie najlepších spermií sa používajú akustické vlny a mikrofluidné zariadenia, ktoré umožňujú šetrnejšie získavanie vhodných spermií.
Identifikácia Relevantných Klinických Dát
Rovnako je výzvou identifikovať správnu kombináciu relevantných klinických dát o stave pacientky.
Inovatívne Metódy a Technológie vo Výskume IVF
Výskum v oblasti umelého oplodnenia neustále napreduje a prináša nové metódy a technológie, ktoré zvyšujú šance párov na úspešné počatie. Medzi najvýznamnejšie inovácie patria:
Využitie miRNA Molekúl ako Ukazovateľov Kvality Embrya
MiRNA molekuly sú RNA molekuly, ktoré sú oveľa kratšie ako DNA a predstavujú kópiu časti DNA, ktorá je v bunke aktívna. MiRNA molekuly sú krátke a nekódujúce a vo väčšine prípadov je ich úloha regulačná, čiže regulujú určité bunkové procesy. Pri štúdiu miRNA molekúl hľadáme také, ktoré dávajú dostatočný signál, aby sme ich mohli využiť v procese výberu embrya. Pochádzajú priamo z embrya, ale získavame ich z tekutiny - kultivačného média, v ktorom sa embryo nachádza, čiže embrya sa vôbec nedotýkame.
Predimplantačný Genetický Skríning (PGS)
Áno, aj na Slovensku, aj v zahraničí je možné využiť služby centier asistovanej reprodukcie predimplantačného genetického skríningu, pri ktorom je možné odsledovať vybrané genetické ochorenia. Je to výhodné, najmä ak je v rodine predispozícia na tieto ochorenia. Týmto spôsobom sa môže z časti eliminovať riziko nevyliečiteľnej choroby.
Využitie Umelá Inteligencia (AI)
Pri výskume ste využili aj umelú inteligenciu. Veľmi nám pomohla v odlíšení a nakombinovaní biomarkerov - molekúl, ktoré nám umožňujú vybrať vhodné embryo. Výhodou je, že umelá inteligencia dokáže obsiahnuť veľké množstvo rôznorodých dát, ku ktorým môžeme pridávať ďalšie parametre. Nie vždy to posilní výpovednú hodnotu, ale umožňuje to poukázať na kľúčové premenné. Sú postupy, ktorými sa viem veľmi priblížiť k výsledku umelej inteligencie, ale AI mi umožňuje spojiť rôzne typy dát a vtedy je jej pridaná hodnota oveľa väčšia.
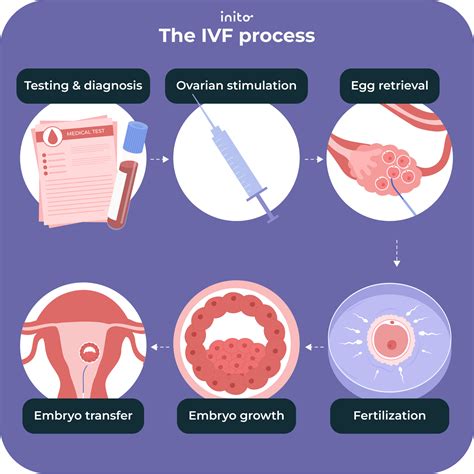
Proces Umelého Oplodnenia (IVF)
Proces IVF je komplexný a zahŕňa niekoľko kľúčových krokov:
Príprava a Stimulácia Vaječníkov
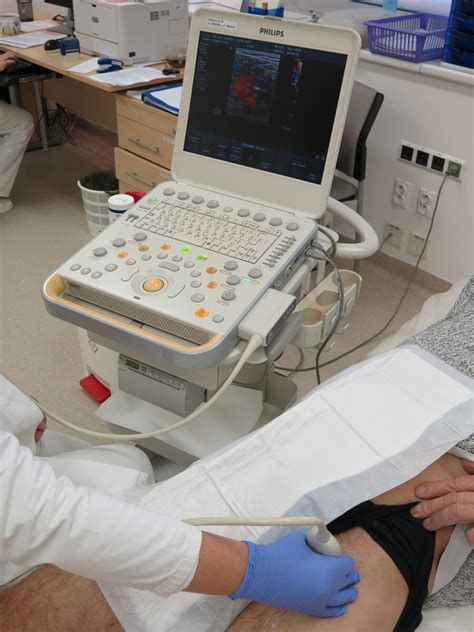
Niektoré pacientky budú potrebovať používanie kontraceptív za účelom časového odsledovania a nastavenia menštruačného cyklu. Taktiež sú kontraceptíva v ART využívané na predchádzanie vzniku ovariálnych cýst, ktoré sa niekedy objavia pri stimulácii GnRH dráhy. V čase očakávaného začatia menštruačného cyklu sa vykoná základné vyšetrenie vaječníkov. Ak by bola viditeľná cysta, väčšinou sa počká s ďalšími krokmi ART, pokiaľ sa cysty nevstrebú (väčšinou v priebehu jedného týždňa). Ojedinele sa môže vykonať drenáž. Vo všeobecnosti sa začína so stimuláciou vaječníkov po začatí menštruačného krvácania. Využité sú viaceré liečivá stimulujúce rast folikulov. Jedná sa o agonisty GnRH receptorov - liečivá zo skupiny gonadotropínov. Druhou skupinou liečiv sú antagonisty GnRH receptorov používané na potlačenie ovulácie nezrelých vajíčok. Na stimuláciu vaječníkov sa využíva viacero rôznych postupov, pričom všetky viac-menej zahŕňajú používanie rovnakého typu liečiv. Pri stimulácii vaječníkov je - dá sa povedať normálnym resp. očakávaným prejavom ich zväčšenie, ktoré časom ustúpi. Avšak veľkým rizikom je vznik ovariálneho hyperstimulačného syndrómu (OHSS), kedy dochádza k nápadnému zväčšeniu vaječníkov, vysokej hladine pohlavných steroidných hormónov v sére a zvýšenej permeabilite ciev, čo môže viesť k akumulácii tekutiny v brušnej, hrudnej a zriedkavo aj v perikardiálnej dutine (dutine okolo srdca). Medzi prejavy OHSS patrí abdominálna (brušná) bolesť či diskomfort, pri ťažších prejavoch sa objavuje nevoľnosť, vracanie či ascites. V prípade vážnych prejavov OHSS je možné sledovať prírastok na váhe, dyspnoe alebo oligúriu (zníženie vylučovanie moču), nerovnováhu elektrolytov, hypovolémiu (znížený objem), pleurálny (pľúcny) výtok až akútnu pulmonálnu úzkosť. Rast folikulov je odsledovaný na základe vaginálneho ultrazvuku v kombinácii s krvnými testami na zistenie hladín hormónov. Takéto testy sa počas celého procesu ART vykonávajú dosť často a na základe nich sa upravuje dávka liečiv za účelom zlepšenia rastu folikulov.
Odber Vajíčok
Tento krok sa vykonáva, aby sa predišlo ovulácii pred tým, než sú vajíčka chirurgicky odobraté lekárom. Pacientke sú podávané buď agonisty, alebo antagonisty GnRH receptorov. Hormón hCG (choriogonádotropný hormón) vo forme liečiv sa používa na finálne dozretie vajíčok. V rámci ART je veľmi dôležité určenie dňa začatia podávania hCG hormónu, pretože od toho sa odvíja čas, kedy sa vajíčka následne budú odoberať. V niektorých postupoch využívajúcich GnRH antagonisty sa na finálne dozrievanie vajíčok využívajú GnRH agonisty. Odber vajíčok sa vykonáva spravidla 32-36 hodín po podaní hCG hormónu. Anesteziológ intravenózne podá liečivá (sedatíva a lieky proti bolesti) na zníženie diskomfortu počas procedúry. Na zobrazenie vaječníkov a jednotlivých folikulov sa používa transvaginálna ultrazvuková sonda. Následne sa ku každému folikulu dovedie dlhá ihla, do ktorej sa nasaje okolitý obsah pozostávajúci z folikulárnej tekutiny, vajíčok (oocytov) a granulóznych (podporných) buniek. Po odbere je pacientka prebratá z anestézie a sledovaná lekárskym personálom, kým anestézia neodznie. Počet odobratých vajíčok závisí od počtu vaječníkov, ich dostupnosti a počtu folikulov, ktoré úspešne odpovedali na stimuláciu. Ultrazvukové zobrazenie poskytuje len približný pohľad na počet odobratých vajíčok. Tento krok spolu so stimuláciou vaječníkov sa spája u žien s náročným obdobím spojeným s nárastom depresií a stavov úzkosti.
Získanie a Spracovanie Spermií
Aby sa zabezpečilo získanie spermií v optimálnej kvalite, je dôležité, aby pacienti nasledovali inštrukcie jednotlivej kliniky. Najčastejšou metódou získania spermií je masturbácia partnera v deň, v ktorý sa uskutočňuje odber vajíčok u partnerky. Príležitostne sa získajú spermie počas súlože so špeciálnym kondómom alebo skrz elektroejakuláciu.
Oplodnenie a Kultivácia Embryí
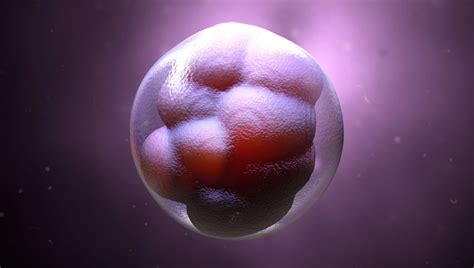
Po odobratí sú vajíčka prenesené do laboratória, kde im sú poskytnuté podmienky vhodné na ich rast. Už pár hodín po odbere sú k nim v miskách umiestnené spermie alebo, v niektorých prípadoch, je injekčne vložená jedna spermia priamo do zrelého vajíčka takzvanou ICSI (intracytoplasmic sperm injection) technikou. ICSI je využívaná najmä v prípadoch porúch mužskej plodnosti. Na druhý deň po oplodnení vajíčok sa sleduje úspešnosť každého jedného vajíčka. Pri normálnom vývoji je možné sledovať prítomnosť dvoch jadier v jednej bunke nazývanej zygota. Po dvoch dňoch sú prítomné už štyri bunky a po troch dňoch už osem buniek. Po piatich dňoch sa zygota vyvinie do štádia blastocysty a následne štádia embrya obsahujúceho 80 a viac buniek malého zárodku človeka. Embryá sú umiestnené v malých miskách alebo skúmavkách s výživným médiom, ktoré im poskytuje podmienky podobné, ako sú vo vajcovodoch či v maternici. Je dôležité poznamenať, že keďže je mnoho vajíčok a embryí abnormálnych, je normálne očakávať, že nie všetky vajíčka budú úspešne oplodnené a nie všetky embryá sa budú deliť normálnym tempom. Šanca, že rozvíjajúce sa embryo skončí tehotenstvom je spojená s jeho rozvojom v laboratóriu, avšak prepojenie nie je stopercentné. To znamená, že nie všetky embryá, ktoré sa delia normálnym tempom, sú geneticky normálne a všetky tie, ktoré sa delia horšie, sú geneticky abnormálne. Napriek tomu je kritériom vo výbere vhodného embrya pre transfer len ich vizuálny vzhľad, ktorý opäť posudzuje pracovník v laboratóriu. Teda opäť sa dá sledovať výrazný zásah do prirodzeného vzniku života.
Prenos Embrya do Maternice
Embryá sú často prenášané do maternice tri až šesť dní po oplodnení. Niekedy sa na transfer používajú trojdňové embryá, ktoré môžu pozostávať zo šiestich až ôsmych buniek. Po prenose takéhoto embrya sa musí ďalej vyvíjať do štádia blastocysty (dutá guľa s približne 100 bunkami), aby mohlo dôjsť k implantácii. Tento vývoj trvá niekoľko dní. Bezprostredne pred implantáciou sa musí blastocysta oslobodiť z obalu, ktorý pôvodne obaľoval vajíčko. Tesne pred prenosom embryí sa na uľahčenie uchytenia sa do priestoru tohto obalu (zona pellucida), ktorý obklopuje vyvíjajúce sa embryá, vytvorí diera a pomocou kyslého roztoku, jemnej ihly alebo laseru sa rozpustí časť tohto obalu. Vyškolení pracovníci, ktorí používajú špecializované nástroje na mikromanipuláciu, to musia vykonať pod mikroskopom. Preimplantačná genetická diagnostika (PGD) a preimplantačná genetická kontrola (PGS) sú dve ďalšie techniky, ktoré sa niekedy používajú počas IVF. Slúžia na testovanie genetických porúch embryí pred ich prenosom do maternice. PGD a PGS umožňujú párom alebo jednotlivcom s vážnymi dedičnými poruchami znížiť riziko, že dieťa bude postihnuté rovnakým problémom. Obidve tieto techniky zahŕňajú použitie mikromanipulátora na odobratie bunky z embrya. Táto bunka je potom odoslaná do diagnostického laboratória na stanovenie normálnosti embrya. Postup prenosu embryí sa zvyčajne vykonáva tri až päť dní po odbere a oplodnení vajíčok. Najväčší vplyv na výsledok tehotenstva majú vek ženy a vzhľad vyvíjajúceho sa embrya. Lekár opatrne zavedie katéter cez krčok do maternice a vloží embryá do dutiny maternice spolu s veľmi malým množstvom tekutiny. Kvalita embryí na prenos je primárne určená na základe morfológie a rýchlosti vývoja v jednom určenom bode - napr. na piaty deň od oplodnenia. Lekári často uprednostňujú takzvaný simulovaný transfer, ktorý sa môže vykonať mesiac pred samotným začatím IVF, počas odberu vajíčok alebo tesne pred samotným skutočným transferom. Ide o procedúru, kedy si lekár nacvičí transfer, zistí aký katéter má použiť, všíma si anatómiu ženy a hľadá najlepší spôsob, ako sa cez krčok dostať do maternice. Ide o simulovaný transfer bez použitia embryí. Simulovaný ani reálny transfer zvyčajne nevyžadujú anestéziu a pacientka zvyčajne opúšťa kliniku po krátkom zotavovacom období. Počet prenesených embryí ovplyvňuje mieru tehotenstva, prípadne viacnásobnú graviditu.
Zmrazovanie Embryí
Zmrazovanie embryí je dôležitou súčasťou procesu IVF. Pacientky, ktoré majú ďalšie kvalitné embryá, ich môžu zmraziť na budúce použitie. Embryá, ktoré spĺňajú vývojové kritériá vzhľadu a rýchlosti rastu, môžu byť zmrazené v ktorejkoľvek z fáz vývoja. Existujú 2 spôsoby, ako zmraziť embryá. Jeden sa nazýva pomalé chladenie. Týmto spôsobom sa embryá umiestňujú do špeciálnych zmrazovacích roztokov a pomocou počítača sa teplota embryí pomaly znižuje. Druhá technika zmrazenia embryí sa nazýva vitrifikácia. Pri tejto ultrarýchlej zmrazovacej metóde sa embryá umiestnia do špeciálnych roztokov a potom sa okamžite premiestnia do tekutého dusíka. Embryá sa následne skladujú tiež v tekutom dusíku. Metóda použitá na zmrazenie embryí rozhoduje o spôsobe ich prípadného rozmrazenia. Nie všetky embryá však proces zmrazenia/rozmrazenia prežijú a niekedy ich po zmrazení dokonca embryo nemožno nájsť. Embryá však môžu byť skladované donekonečna bez zjavného poškodenia ich kvality. V súčasnosti majú reprodukčné kliniky veľký problém so skladovaním takýchto zamrazených embryí. Podľa viacerých dát len v Spojených štátoch je uskladnených viac ako milión zamrazených embryí.
Tehotenský Test a Následná Starostlivosť
Úspešné uchytenie sa embrya v sliznici maternice závisí od primeranej hormonálnej podpory. Na tento účel sa používa najmä orálne, intramuskulárne alebo vaginálne podávaný progesterón. Denné používanie bude pokračovať až do tehotenského testu. Tehotenský test je potrebné vykonať 9 až 12 dní po prenose embrya bez ohľadu na vaginálne špinenie alebo krvácanie. Ak je výsledok testu pozitívny, zvyčajne sa opakuje ešte o 2 dni neskôr. Je potrebné dôkladne sledovať tehotenstvo, aby sa odhalil prípadný potrat alebo mimomaternicové tehotenstvo a aby sa mohli riešiť viacnásobné tehotenstvá. Pacientky sú zvyčajne prepustené z kliniky do rúk svojho ambulantného gynekológa v 8. až 10. týždni tehotenstva.
Úspešnosť Umelého Oplodnenia a Porovnanie s Prirodzeným Oplodnením
Na Slovensku sa úspešnosť IVF pohybuje okolo 60 %, zahraničné centrá asistovanej reprodukcie uvádzajú približne rovnaké čísla. Najvyššiu deklarovanú úspešnosť IVF som našla v Los Angeles, kde uvádzajú až 88 %, ale je otázne, či je to pravda. Závisí to aj od toho, čo všetko je do štatistiky zahrnuté, avšak keďže každé pracovisko spracováva a vyhodnocuje výsledky odlišným spôsobom, nie je možné ich priamo porovnávať. Dôležitejšia by však bola štatistika, koľko tehotenstiev sa skončí narodením dieťatka. Vplyv má, samozrejme, pripravenosť matky aj otca a samotný výber embrya.
Vedci odporúčajú ženám, aby zvážili riziká spojené s in vitro fertilizáciou, intracytoplazmatickou injekciou spermie či vyvolaním ovulácie. Deti, ktoré prišli na svet vďaka asistovanej reprodukcii, majú podľa vedcov z Adelaidskej univerzity väčšie sklony k zdravotným poruchám. Metódy ako vyvolanie ovulácie, in vitro fertilizácia alebo vloženie spermie do vajíčka viedli k vážnym poruchám u 8,3 percenta zo sledovaných detí. Pri prirodzenom oplodnení vedci hovoria o 5,8 percenta prípadov, čo je podľa vedúceho výskumu Michaela Daviesa z Robinsonovho inštitútu pre plodnosť veľmi výrazný rozdiel. „Mám podozrenie, že risk splodenia chorého dieťaťa je niečo, o čom sa pravdepodobne na klinike často nehovorí. Takže týmto zdôrazňujeme, že ide o vec, o ktorej pacienti a lekári musia diskutovať," vyjadril sa. Podľa Daviesa sa pri výskume sústredili na vážne poruchy, ktoré "si buď vyžadujú liečbu, alebo liečba neexistuje a deti sú považované za postihnuté." Spomenul napríklad srdcové poruchy či mozgovú obrnu.
Rozdiely Medzi Metódami Asistovanej Reprodukcie
Ukázalo sa však, že nie všetky spôsoby liečby neplodnosti sú rovnako riskantné. Po in vitro fertilizácii sa 7,2 percenta detí narodilo s poruchami, pričom číslo sa ešte zvyšovalo s vekom rodičov či ich fajčením. Pri intracytoplazmatickej injekcii spermie to bolo až 9,9 percenta detí. Podľa Daviesa dôvodom môže byť používanie menej kvalitných spermií či skutočnosť, že spermie a vajíčka sa manipuláciou v laboratóriu môžu poškodiť. Pri in vitro fertilizácii percento môže byť nižšie preto, že spermiu do vajíčka nevkladajú, ale prenikne do neho sama. Vedci zároveň upozorňujú na lieky na vyvolanie ovulácie s účinnou látkou clomiphene citrate, ktoré podľa nich strojnásobujú pravdepodobnosť narodenia chorého dieťaťa.
Kmeňové Bunky a Ich Potenciál v Reprodukčnej Medicíne
Kmeňové bunky majú potenciál konat zázraky. Výskum kmeňových buniek ešte nepokročil natolik, aby sme boli schopní vypestovať náhradný orgán pre transplantáciu. Ničmenej tu môžu pomôcť techniky asistovanej reprodukcie. Tie pomôžu deťom vyliečiť smrteľné ochorenie, ktoré sa dá liečiť transplantáciou kmeňových buniek z kostnej drene. Asistovaná reprodukcia môže pomôcť tým, že budú pripravené embryá od rovnakých rodičov a pred implantáciou do maternice sa u nich vykoná preimplantačná genetická diagnostika - savior sibling (výraz pre dieťa, ktoré sa narodí za pomoci umelého oplodnenia kvôli zaisteniu buniek či orgánov pre smrteľne chorého súrodenca). Na základe výsledku sa pre implantáciu vyberie to embryo, ktoré je kompatibilné s chorým súrodencom a netrpí danou mutáciou. Pri narodení sa odoberie pupočníková krv a z nej sa izolujú kmeňové bunky, ktoré sa použijú pre transplantáciu u chorého súrodenca.
Embryonálne a Indukované Pluripotentné Kmeňové Bunky
Embryonálne kmeňové bunky sú získané z tzv. "nadbytočných" embryí, počatých prostredníctvom techník umelého oplodnenia a zanechaných na použitie vo výskume. Zamrazené embryá sa nechajú rozmraziť a vyvíjať 6 až 7 dní do štádia blastocysty. Indukované pluripotentné kmeňové bunky pochádzajú z tela dospelého človeka (napríklad z jeho kože), avšak sú preprogramované, aby sa znovu stali nediferencovanými kmeňovými bunkami. Potom sú nasmerované tak, aby sa vyvinuli do želaných typov tkaniva.
Terapia Bunkami a Jej Aplikácie
Terapia bunkami je transplantácia alebo implantácia buniek, ktorej zámerom je obnoviť funkciu nejakého tkaniva alebo orgánu, ktorý bol poškodený. Dospelé kmeňové bunky sa už teraz používajú na liečenie ochorení krvi (formy leukémie), na liečenie rán a popálenín, na opravu poškodených šliach a na výrobu tkanív (obnovenie trachey). Niektoré dospelé kmeňové bunky, predovšetkým tie, ktoré pochádzajú z pupočníkovej krvi, umožňujú obnovenie buniek v stenách ciev. Aj keď tieto spôsoby liečenia rozličným spôsobom profitovali z pokroku v oblasti kmeňových buniek a zdajú sa byť sľubné pre tzv. Ľudské embryonálne kmeňové bunky a indukované pluripotentné kmeňové bunky sa používajú na liečenie pacientov v rámci klinických pokusov. Slúžia na modelovanie ochorení a výskum molekúl užitočných pre farmaceutický výskum.
Prelomové Obavy a Budúcnosť Výskumu
What are stem cells? - Craig A. Kohn
Vytváranie Ľudských Vajíčok z Kožných Buniek
Vedci vytvorili ľudské vajíčka z kožných buniek a oplodnili ich spermiou. Vedcom v Spojených štátoch sa podaril doslova prelomový objav, ktorý môže zmeniť pohľad na plodnosť a plánovanie rodičovstva. Po prvý raz v histórii sa im podarilo vytvoriť oplodniteľné ľudské vajíčka z bežných kožných buniek namiesto vaječníkov.
Proces Vytvárania Vajíčok z Kožných Buniek
Tradične vzniká nový život spojením vajíčka a spermie. V prípade novej technológie je tomu však inak. Tím z Oregonskej univerzity najprv odobral jadro z kožnej bunky, ktoré obsahuje kompletný genetický kód človeka. Toto jadro vložili do darovaného vajíčka, z ktorého predtým odstránili jeho pôvodné jadro. Výsledkom bol hybridný „základ“ nového vajíčka. Tu však nastal zásadný problém. Preto vedci vyvinuli špeciálny proces, ktorý nazvali „mitomeióza.“ V ňom skombinovali dva typy bunkového delenia odborne označované ako mitóza a meióza.
Výsledky Experimentu
Výsledkom experimentu bolo 82 vyvíjajúcich sa vajíčok, ktoré následne vedci oplodnili spermiou v laboratóriu. Zhruba 9 percent z nich sa vyvinulo do raného embryonálneho štádia a teoreticky by tak mohli byť implantované do maternice. Ani jedno embryo sa však nevyvíjalo dlhšie než šesť dní. Vedci zároveň upozorňujú, že mnohé z nich mali genetické abnormality. „Dosiahli sme niečo, čo sa dlho považovalo za nemožné,“ uviedol profesor Shoukhrat Mitalipov. Zároveň však priznáva, že technológia potrebuje roky ďalšieho výskumu, kým bude bezpečná a spoľahlivá. Navyše, technológia nepotrebuje ženskú kožnú bunku. Teoreticky je možné vytvoriť vajíčko aj z mužskej kožnej bunky. To otvára dvere párom rovnakého pohlavia, aby mali geneticky spoločné dieťa, napríklad z DNA jedného muža vznikne vajíčko a druhý poskytne spermiu. Vedci upozorňujú, že komerčné využitie tejto technológie je vzdialené minimálne jedno desaťročie. Najväčšou výzvou je, aby vajíčka vytvorené z kožných buniek mali správny počet a štruktúru chromozómov.
Modely Ľudských Embryí
Vedci sa pokúšajú napodobniť počiatky ľudského života, a to bez dvoch nevyhnutných zložiek: spermií a vajíčok. Tieto modely embryí nie sú síce zďaleka dokonalými kópiami, no sú čoraz zložitejšie a začínajú sa nielen podobať na skutočné embryá, ale aj sa správať ako ony. Modely embryí by mohli pomôcť lepšie pochopiť vývin človeka aj príčiny neplodnosti.
Vývin a Potenciál Modelov Embryí
„Nikto z nás netušil, že veda sa posunie tak rýchlo. Je to neuveriteľný, úplne prelomový krok,“ hovorí profesorka Amander Clarková z Kalifornskej univerzity v Los Angeles, odborníčka na bunkovú a vývinovú biológiu a zakladateľka Centra pre reprodukčnú vedu, zdravie a vzdelávanie. Mohli by sme sa dočkať modelu, ktorému by tĺklo srdce alebo ktorý by dokázal cítiť bolesť? Podľa súčasného stavu výskumu zatiaľ neexistuje žiadny model, ktorý by úplne napodobňoval vývin ľudského embrya. A zatiaľ sa nepredpokladá, že by mal ktorýkoľvek z nich potenciál vyvinúť sa do štádia plodu, teda do fázy, ktorá v tehotenstve zodpovedá približne 8. týždňu (56. Vytváranie podobných modelov je navyše nie veľmi úspešné. Väčšine výskumných tímov sa darí len zriedkavo. Iba malá časť kmeňových buniek sa spontánne zorganizuje do štruktúr, ktoré pripomínajú embryo. Napriek tomu však modely vykazujú niekoľko vnútorných znakov a typov buniek, ktoré sú nevyhnutné pre vývin embrya. Ide napríklad o amnión (vnútorný plodový obal), žĺtkový vak či tzv. primitívny prúžok, ktorý je základom vzniku chrbtice. Podľa štúdie, na ktorej sa autorsky spolupodieľala aj profesorka A. Clarková a ktorá vyšla v odbornom časopise Stem Cell Reports, by sa tieto štruktúry - pri ďalšom zlepšení technológie - mohli v budúcnosti vyvíjať ďalej až po embryonálne základy srdca, mozgu a iných orgánov.
Etické a Regulačné Aspekty Modelov Embryí
Je zásadné pochopiť, že cieľom výskumu nie je vytvárať životaschopné plody alebo bytosti schopné ľudského vedomia. Napriek tomu, ako výskum napreduje, hrozí, že sa hranica medzi laboratórnym modelom a skutočným ľudským embryom začne stierať. A práve preto, ako upozorňuje profesorka Clarková, si táto práca vyžaduje oveľa dôslednejší dohľad než iné vedecké disciplíny. V polovici júna Clarková spolu s pracovnou skupinou Medzinárodnej spoločnosti pre výskum kmeňových buniek (ISSCR) špecializujúcou sa na modely embryí odporučili sprísniť dohľad nad výskumom, ktorý sa týka týchto modelov. Smernice ISSCR doposiaľ rozlišovali medzi tzv. integrovanými modelmi...
Etické a Spoločenské Aspekty Asistovanej Reprodukcie
Život v moderné dobe stále častejšie naráža na etické hranice. Dostávame sa do obdobia, kedy poznanie prekročilo hranice toho, čo ľudia dlho považovali za nemožné. Stále častejšie veda otvára nové dvere s úžasnými možnosťami. Zatiaľ čo technický pokrok má len vzácne etické hranice, pokrok v medicíne a biológii na ne naráža takmer vždy. Od chvíle, kedy bol človeku podaný liek, ktorý odvrátil smrteľnú chorobu, zasahujeme do prirodzeného vývoja vecí. Napríklad minulý rok v Číne prebehla súdna žaloba, kedy manžel zažaloval manželku za to, že mu zatajila jej mnohé plastické operácie, ktoré ju skrášlili. Jedným z veľkých etických míľnikov modernej doby bola asistovaná reprodukcia, ktorá umožnila mať vlastné deti aj ľuďom, ktorí prirodzene počať nemohli. Samotná asistovaná reprodukcia je mnohokrát ešte stále zatracovaná a genetika označovaná ako degeneračný zásah do populácie. Predsa sme schopní rozmnožiť ľudí, ktorí by sa prirodzene množiť nemali. V tomto kroku sa ale dostávame do kríža so základnými ľudskými právami, ako ich deklaruje ústava. Kde sú hranice toho, čo by sme mali urobiť, aby sme pomohli jednotlivcovi a neohrozili budúce generácie? Etické pravidlá sú veľmi krehké a vyplývajú z názoru väčšiny. Väčšina určuje to, čo je správne vykonávať a čo bude zatracené. Vždy sa budete pozerať na etický problém podľa svojej skúsenosti. Ak sa ich daný problém netýka, má väčšina ľudí tendenciu byť proti. Ak by ale nejaký postup mohol pomôcť vyriešiť vašu ťažkú životnú situáciu, budete sa na neho pozerať celkom opačne.
"Dieťa na Objednávku" a Savior Sibling
Niektorí ľudia sa na tento počin pozerajú ako na umelé vytváranie detí a obávajú sa o ich psychologický vývoj v detstve, kedy by s nimi mohlo byť zaobchádzané ako s nadbytočným dieťaťom. Napriek tomu rodiny, ktoré takto dieťa počali, uviedli, že si rovnako želali ďalšieho potomka. Verím, že pohľad ľudí sa radikálne mení s tým, na akej strane sa ocitnú. Ukážkou toho je spoločnosťou dlho odsudzované „dieťa na objednávku". Napríklad Jamie Whitaker. Jamie sa narodil v roku 2003 a ešte keď bol embryo, jeho rodičia do neho vkladali veľké nádeje na uzdravenie jeho staršieho brata Charlieho. U Charlieho sa prejavila fatálna Diamond-Blackfan anémia a bez komplementárneho darcu kostnej drene bolo len otázkou času, kedy zomrie. Keďže Charlie v tom čase nemal žiadneho súrodenca, jednou z nádejí bolo počatie súrodenca, ktorý by mal zhodu v HLA typizácii (HLA majú významnú funkciu v imunitnom systéme človeka). Tu zasiahla asistovaná reprodukcia, ktorá umožnila prípravu šiestich embryí a ich následnú preimplantačnú diagnostiku, vďaka ktorej bola nájdená zhoda HLA u troch embryí. Dve vyšetrené embryá boli zavedené a narodil sa Jamie. Neskôr sa pupočníková krv mladšieho brata použila na transplantáciu a v roku 2012 bol Charlie diagnostikovaný ako uzdravený. Ďalšou možnosťou, ako reprodukčná medicína môže pomôcť s ďaleko menším dopadom na spoločnosť, je použitie nevyužitého, nadbytočného embrya pre kultiváciu špecifickej tkane a orgánu. V podstate možno využiť tento prístup iba u detí, ktoré boli počaté takzvane v skúmavke, alebo ktorých súrodenci boli takto počatí.
Obavy z Genetických Manipulácií
Ľudia sa obávajú detí na objednávku. Obávajú sa toho, že raz pokročí doba natoľko, že budeme schopní manipulovať s genetickou informáciou a vytvoriť tak jedinca požadovaných kvalít. V súčasnej dobe sme na míle vzdialení takým predstavám, ale nemožno vylúčiť, že v budúcnosti budeme schopní zasahovať do genómu ľudí.
Budúcnosť Reprodukčnej Medicíny
Neplodnosť trápi až 20 percent párov. Aj keď medicínsky odbor asistovanej reprodukcie dosiahol od narodenia Louise Brownovej obrovský pokrok, stále nedokáže pomôcť všetkým. Vedci však usilovne pracujú na tom, aby týmto ľuďom chýbajúce pohlavné bunky vypestovali v laboratóriu. Ich postup pripomína techniku, ktorou v roku 1996 priviedli škótski vedci na svet ovcu Dolly, teda prvého klonovaného cicavca. Mitalipov a spol. využili to, že sa vajíčko pri oplodnení zbaví polovice dedičnej informácie, aby bolo schopné prijať dedičnú informáciu spermie. Pri klonovaní je pri vajíčku spojenom s telesnou bunkou nastavený vývoj na embryo. Mitalipov a jeho spolupracovníci však vajíčko nesúce dedičnú informáciu kožnej bunky oplodnili spermiou. Vzniklo tak embryo, ktoré nie je genetickou kópiou darcu kožnej bunky, ako je to v prípade klonov. Napriek obavám, ktoré zavládli po narodení ovce Dolly, sa nikto do klonovania ľudí nepustil. Jedným z dôvodov je obava z vrodených defektov, ktorými bývajú klony zvierat postihnuté.

tags: #embryo #kmenove #bunky #vyskum #asistovana #reprodukcia