Vnútromaternicová rastová retardácia (IUGR) je významný zdravotný stav, ktorý ovplyvňuje vývoj plodu počas tehotenstva. Ide o situáciu, keď plod nedorastie do očakávanej hmotnosti a veľkosti, čo môže viesť k rôznym komplikáciám pre dieťa aj matku. Pochopenie IUGR je kľúčové pre nastávajúcich rodičov aj poskytovateľov zdravotnej starostlivosti, pretože včasná detekcia a liečba môžu výrazne zlepšiť výsledky u postihnutých detí. Vnútromaternicové obmedzenie rastu je komplexný stav, ktorý môže mať významné dôsledky pre matku aj dieťa. Pochopenie príčin, symptómov, diagnostiky, možností liečby a preventívnych stratégií je kľúčové pre nastávajúcich rodičov a poskytovateľov zdravotnej starostlivosti.
Vnútromaternicová rastová retardácia (IUGR) je definovaná ako stav, pri ktorom plod nie je schopný dosiahnuť svoj geneticky predurčený rastový potenciál. Tento stav sa zvyčajne diagnostikuje, keď je hmotnosť plodu nižšia ako 10. percentil pre jeho gestačný vek. IUGR možno rozdeliť na dva hlavné typy: symetrickú a asymetrickú. K IUGR môže prispieť niekoľko infekčných agensov a faktorov prostredia. Genetické faktory môžu tiež zohrávať úlohu pri IUGR. Niektoré dedičné ochorenia môžu predisponovať plod k rastovým obmedzeniam.
Životný štýl matky a stravovacie návyky významne ovplyvňujú rast plodu. IUGR nemusí vždy prejavovať zjavné príznaky počas tehotenstva. Medzi bežné príznaky patrí znížený pohyb plodu, malá výška fundusu a abnormálne ultrazvukové nálezy.
Vnútromaternicová rastová retardácia (IUGR) patrí medzi bežné komplikácie tehotenstva s možnými závažnými dopadmi na vývoj plodu a dieťaťa. Predovšetkým v dôsledku komplikovanej definície nie je početnosť tejto tehotenskej patológie presne známa, nakoľko sa odhaduje, že postihuje až 10 % všetkých tehotenstiev. Spoločne s predčasným pôrodom (nezrelosťou) predstavuje IUGR najčastejšie patologické stavy vedúce k novorodeneckej morbidite (chorobnosti) a mortalite (úmrtnosti).
Všeobecne akceptovaná definícia IUGR neexistuje. Diagnostika vychádza z ultrazvukom zaznamenaného výrazného spomalenia rastu plodu. Inými slovami, plod v maternici po období normálneho rastu svoj ďalší rast významne spomaľuje a odchyľuje sa od geneticky predpokladanej rastovej rýchlosti. Rozlišujeme dve základné situácie: 1) plod rastie veľmi zle už od začiatku gravidity, alebo 2) rast plodu sa začína spomaľovať v 2. alebo 3. trimestri (tretine) tehotenstva. V oboch prípadoch je situácia závažná, hoci jej príčina býva rozdielna.
Ak plod rastie zle už od samého začiatku tehotenstva a celé telíčko plodu je súmerné, potom je možné, že príčina pomalého rastu plodu tkvie v genetickej poruche pri utváraní zárodku a plod nemá normálnu genetickú informáciu. Vyšetrenie tzv. karyotypu z pupočníkovej krvi alebo plodovej vody môže priniesť kľúčovú informáciu vysvetľujúcu dôvod neadekvátneho rastu plodu. Ďalšou možnosťou nápadne pomalého rastu plodu už od 1. trimestra sú niektoré vrodené vývojové vady, vrodené infekcie alebo zriedkavejšie napríklad abnormálne utváraná či malá placenta.
Častejšie je však spomalenie rastu plodu až neskôr v priebehu gravidity. Tu je typickou príčinou tzv. placentárna nedostatočnosť, kedy placenta prestáva plniť svoju úlohu v zabezpečení dodávky kyslíka a živín plodu v dôsledku celej rady situácií (bežne hypertenzia, preeklampsia, tehotenská cukrovka alebo napríklad fajčenie tehotnej). V rámci maximálneho šetrenia kyslíkom a živinami plod znižuje svoje metabolické nároky (prestáva rásť a prestáva sa hýbať), dochádza k prioritnému smerovaniu toku okysličenej krvi do mozgu, srdca a nadobličiek, a naopak sa znižuje zásobenie obličiek, celého tráviaceho traktu vrátane pečene, svalov, kostí, kože… Srdce plodu začína pracovať v podmienkach veľkej záťaže (nedostatku kyslíka).
V dôsledku zníženého prekrvenia obličiek sa znižuje produkcia moču plodu, ktorý tvorí v 2. polovici tehotenstva viac ako dve tretiny plodovej vody, a tak pôrodník pri ultrazvukovom vyšetrení môže zistiť, že v maternici chýba plodová voda. Ak je táto situácia identifikovaná v neskorších fázach tehotenstva (čo je paradoxne niekedy obtiažnejšie), je veľmi žiaduce nevystavovať plod takémuto nepriaznivému prostrediu a tehotenstvo plánovane ukončiť, keďže adekvátne množstvo kyslíka (a živín) v inkubátore je pre bábätko bezpečnejšie a dieťa je možné navyše trvalo monitorovať.
Veľký problém nastáva v situácii, keď dochádza k rastovému oneskoreniu už v priebehu 2. tretiny gravidity a pôrodníci spoločne s neonatológmi musia balansovať riziká pokračovania tehotenstva (a hroziaceho rizika úmrtia plodu v maternici) proti rizikám predčasného pôrodu a závažnej nezrelosti.
Následky IUGR môžu znamenať riziko rozvoja akútnych aj celoživotných komplikácií. Čoskoro po narodení býva problematická funkcia gastrointestinálneho traktu s poruchami trávenia a odchodu stolice, nízkou hladinou krvného cukru (glykémie) a rizikom nekrotizujúcej enterokolitídy. V dlhodobejšom horizonte (roky) sa stretávame predovšetkým s poruchami psychomotorického vývoja a poruchami rastu. V horizonte najvzdialenejšom (roky - desiatky rokov) je možné očakávať zhoršujúcu sa funkciu obličiek, hypertenziu a sklon k rozvoju tzv. metabolického syndrómu (obezita, cukrovka 2. typu, ateroskleróza, ischemická choroba srdca…). Pravdepodobnosť rozvoja všetkých týchto stavov je závislá predovšetkým od závažnosti IUGR, dĺžky expozície nepriaznivým vnútro maternicovým podmienkam a komplikáciám, ktoré sa odohrajú po narodení.
Zďaleka najhoršia situácia však nastáva v situácii, keď závažná IUGR pri nedostatočnej funkcii placenty nie je v priebehu tehotenstva rozpoznaná. Prehlbujúci sa nedostatok kyslíka vedie k vnútro maternicovému úmrtiu plodu alebo k rozvoju srdcového zlyhania. V tejto situácii sú všetky ďalšie orgány plodu vystavené ďalšiemu závažnému nedostatku kyslíka. Dochádza k rozvoju tzv. hypoxicko-ischemického postihnutia mozgu, bohužiaľ pri pridruženom postihnutí pečene a kostnej drene niekedy navyše súčasne s krvácavými komplikáciami. Pôrod dieťaťa v takto závažnom stave (multiorgánové zlyhanie) je veľmi zložitou situáciou s neistým výsledkom v zmysle prežitia a predovšetkým v zmysle dlhodobej prognózy. Bohužiaľ takto závažná situácia môže nastať v dôsledku zložitosti tejto problematiky aj dnes.
Vývoj embrya je zložitý a citlivý proces, ktorý môže byť ovplyvnený mnohými faktormi. Pomalý vývoj embrya, alebo dokonca zastavenie vývoja, je pomerne častým javom, najmä v kontexte asistovanej reprodukcie. Tento článok sa zameriava na možné príčiny pomalého vývoja embrya a faktory, ktoré môžu tento proces ovplyvniť.
Od momentu oplodnenia vajíčka spermiou začína proces kultivácie embrya. Embryo je "sledované" v laboratórnych podmienkach počas 3 až 5 dní, kým je pripravené na vklad do maternice. Počas tejto doby môže dôjsť k zastaveniu vývoja embrya z rôznych dôvodov. Niektoré kliniky asistovanej reprodukcie používajú embryoskop, ktorý 24 hodín denne monitoruje vývoj embrya a umožňuje presne určiť, kedy a kde nastala chyba vo vývoji.
Existuje niekoľko faktorov, ktoré môžu prispieť k pomalému vývoju embrya:
- Genetické faktory: Najčastejšou príčinou zastavenia vývoja embrya sú genetické abnormality. Tieto abnormality môžu vzniknúť spontánne alebo môžu byť dedičné.
- Kvalita spermií a vajíčok: Zlá kvalita spermií alebo vajíčok môže viesť k pomalému vývoju alebo zastaveniu vývoja embrya. Poškodenie DNA spermií, nízka pohyblivosť alebo koncentrácia spermií môžu negatívne ovplyvniť oplodnenie a vývoj embrya. Zrelosť vajíčka je tiež dôležitá, pričom zrelosť sa určuje pomocou prítomnosti polárneho telieska a deliaceho vretienka.
- Problémy s oplodnením: Ak spermia nemá faktory potrebné na aktiváciu vajíčka (oocytu), proces oplodnenia sa nemusí uskutočniť. Asistovaná aktivácia vajíčka pomocou kalciového ionofóru môže pomôcť v takýchto prípadoch.
- Laboratórne podmienky: Kvalita laboratória a skúsenosti embryológov zohrávajú kľúčovú úlohu v úspešnosti liečby. Moderné prístrojové vybavenie a pravidelné vzdelávanie embryológov sú nevyhnutné pre optimálny vývoj embryí.
- Imunologické faktory: Imunologická nekompatibilita medzi matkou a embryom môže viesť k zastaveniu vývoja embrya.
Vedecký objav z Ústavu živočíšnej fyziológie a genetiky AV ČR osvetlil proces vývoja zdravého embrya. Zistilo sa, že pre zdarný vývoj myšieho zárodku v štádiu dvojbunkového embrya je zásadné predĺženie jednej prípravnej fázy bunkového cyklu. Bol popísaný proteín CHK1, ktorý reguluje dĺžku bunkového cyklu a je kľúčový pre správne načasovanie delenia buniek. Ak tento proteín chýba, embryo sa nevyvinie do blastocysty.
Vývoj embrya po IVF:
- 1. deň po oplodnení: Hodnotí sa výsledok fertilizácie.
- 2. deň po oplodnení: Embryo je tvorené štyrmi bunkami.
- 3. deň po oplodnení: Embryo by malo mať šesť až osem buniek.
- 4. deň po oplodnení: Vzniká morula, bunky sa viac spájajú.
- 5. deň po oplodnení: Embryo je vo štádiu blastocysty a môže byť prenesené do maternice.
- 6. deň po oplodnení: Embryo môže začať tzv. hatching (liahnutie sa z obalu).
Po transferi embrya do maternice nasleduje nidácia, čiže uhniezdenie embrya do sliznice maternice. Embryotransfer (ET) sa vykonáva tenkým katetrom. Môže byť vykonaný v tom istom cykle ako odber oocytov (čerstvý transfer) alebo v neskorších cykloch.
Asistované reprodukčné techniky na podporu vývoja embrya:
- Asistovaný hatching: Narušenie obalu embrya (zona pellucida) laserom na uľahčenie uhniezdenia.
- EmbryoGlue: Kultivačné médium zvyšujúce priľnavosť embrya k sliznici maternice.
Vplyv životného štýlu oboch partnerov môže výrazne ovplyvniť kvalitu spermií a vajíčok, a tým aj vývoj embrya:
- Prestať fajčiť.
- Obmedziť konzumáciu alkoholu.
- Znížiť stres.
- Pravidelne cvičiť.
- Zdravo sa stravovať.
- Udržiavať optimálnu hmotnosť.
Genetické poruchy chromozómov môžu byť príčinou pomalého vývoja embrya a vývojových porúch. Najčastejšie sa vyskytujú chyby v počte chromozómov, ako napríklad Downov syndróm. Vyšší vek matky zvyšuje riziko vzniku vývojovej poruchy.
Prenatálna diagnostika sa venuje skríningu vrodených vývojových porúch ešte v tehotenstve. Výsledky získava spájaním viacerých testov a podrobných ultrazvukových vyšetrení v rôznych týždňoch tehotenstva.
Veľkosť plodu v tehotenstve patrí k faktorom, ktoré môžu vyvolať obavy u tehotných žien. Je dôležité uvedomiť si, že tabuľkové údaje o dĺžke a hmotnosti plodov udávajú priemerné hodnoty pre konkrétny týždeň gravidity.
Rôstová reštrikcia plodu (FGR - fetal growth restriction, tiež označovaná ako intrauterinná rastová retardácia, IUGR - intrauterine growth restriction) je stav, kedy plod v dôsledku patologického procesu nedosahuje svoju geneticky predpokladanú rastovú veľkosť. Najčastejšou príčinou FGR býva patologická funkcia placenty, avšak etiológia môže byť veľmi rozmanitá. Kauzálna liečba rastovej reštrikcie neexistuje. Dôraz sa kladie predovšetkým na prevenciu ovplyvniteľných materských rizikových faktorov, ako je napr. fajčenie, a na pravidelné prenatálne kontroly.
Fetálna rastová reštrikcia (FGR) sa podľa doby svojho výskytu v tehotenstve delí na časnú (early FGR, do 32. týždňa tehotenstva) a neskorú (late FGR, od 32. týždňa tehotenstva). Priemerná veľkosť plodu (EFW) alebo obvod brucha (AC) pod 3. percentilom, alebo pomer EFW/AC pod 10. percentilom môže signalizovať FGR.
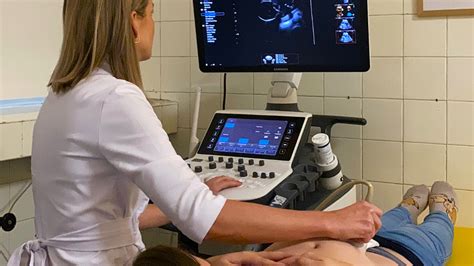
V rámci sledovania rastu a vývoja plodu sa vykonáva ultrazvuková biometria. Vyšetrenie obehu plodu sa vykonáva pomocou dopplerovskej sonografie.
V dospelosti môžu byť následky IUGR spojené s rizikom rozvoja diabetes mellitus 2. typu, hypertenzie a metabolického syndrómu.
Chicken Embryo Development
Pri diagnóze IUGR je nevyhnutné kontaktovať poskytovateľa zdravotnej starostlivosti. Liečba IUGR závisí od základnej príčiny a závažnosti ochorenia. Prognóza pre dojčatá s diagnostikovanou IUGR sa líši v závislosti od niekoľkých faktorov vrátane závažnosti rastového obmedzenia, základnej príčiny a načasovania diagnózy a intervencie.
Tento článok slúži len na informačné účely a nenahrádza odbornú lekársku pomoc.