Placenta, nazývaná aj plodový alebo materský koláč, je dočasný orgán, ktorý počas vnútromaternicového vývinu slúži na látkovú výmenu medzi plodom a matkou. Je pripojená k stene maternice, zvyčajne v hornej alebo bočnej časti. S vyvíjajúcim sa plodom ju spája pupočná šnúra. Placenta zohráva kľúčovú úlohu pri starostlivosti o plod a zabezpečuje jeho blaho. Keď sa dozvedáme viac, náš obdiv k tomuto neuveriteľnému orgánu sa len prehlbuje.
Vývin placenty začína po nidácii blastocysty do endometria maternice. Endometrium, sliznica maternice, v tomto období (20.-21. deň cyklu) je na vrchole sekrečnej fázy. Je hrubé asi 6 mm, presiaknuté tekutinou, dobre prekrvené, s postáčané a rozšírené žliazky produkujúce hlienovitý sekrét. Počas nidácie, asi 3 dni od jej začiatku, dochádza v endometriu k nápadným zmenám nazývaným deciduálna reakcia. Blastocysta produkuje látky podobné hormónom s regionálnym účinkom, na ktoré sliznica reaguje rastom, hrubnutím a deciduálnymi zmenami. V okolí blastocysty sa zmnožujú a vetvia cievy. Väzivové bunky endometria, fibroblasty, sa transformujú na tzv. deciduálne bunky. Tieto zmenené bunky majú polyedrický tvar, sú zväčšené, s vakuolizovanou cytoplazmou, ktorá obsahuje veľa glykogénu a lipidov. Takto zmenená sliznica maternice sa nazýva decidua a je pripravená na začínajúcu sa graviditu. Po skončení nidácie, približne od konca 2. týždňa po oplodnení, sa sliznica maternice delí na štyri topografické oblasti: decidua basalis - pod nidovanou blastocystou, najhrubšia časť, zúčastňuje sa na vývine placenty. decidua marginalis - po stranách blastocysty. decidua capsularis - nad blastocystou smerom do dutiny maternice. decidua parietalis - ostatná sliznica maternice.
Súčasne s deciduálnymi zmenami prebieha diferenciácia buniek blastocysty. Vonkajšia stena blastocysty, trofoblast, sa po kontakte so sliznicou maternice rozdeľuje na dve časti: vnútornú - cytotrofoblast a vonkajšiu - syncýtiotrofoblast. Bunky cytotrofoblastu sa neustále delia a ich bunkové membrány zanikajú, čím vzniká mnohojadrový cytoplazmatický útvar - syncýcium. Rast syncýtiotrofoblastu je intenzívnejší v oblasti decidua basalis. V histiotrofnom štádiu výživy embrya syncýtiotrofoblast vytvára výbežky do okolitej sliznice. Pôsobením proteolytických enzýmov rozrušuje žliazky, cievy a tkanivo sliznice. Výživné látky z rozrušenej sliznice prechádzajú cez syncýtiotrofoblast a cytotrofoblast do buniek embrya. V lakunárnom štádiu vývinu trofoblastu (10.-12. deň vývinu) sa v syncýtiotrofoblaste tvoria vakuoly, ktoré splývajú do dutiniek - lakún. Spájanie susedných lakún vytvára komunikačnú sieť priestorov, ktoré sa neskôr stanú budúcimi medziklíkovými (intervilóznymi) priestormi. Do týchto priestorov preniká sekrét zo žliazok a krv z porušených kapilár sliznice. V trabekulárnom štádiu vývinu trofoblastu sa lakúny rozdeľujú syncýtiotrofoblast na trabekuly (trámce). V hemotrofnom štádiu výživy krv matky z uterinných artérií preteká do lakún a obmýva tieto trámce syncýtiotrofoblastu. Výživné látky prechádzajú priamo z krvi matky do buniek embrya cez trofoblast, čo tvorí základ uteroplacentárnej cirkulácie.
Koncom 2. a v 3. týždni vývinu z choriovej blany vyrastajú choriové klky (villi choriales). Choriová blana, ktorá sa vyvíja z trofoblastu, intenzívne rastie od 9. do 25. dňa vývinu. Po celom povrchu choriovej blany vyrastajú bunkové stĺpce cytotrofoblastu, ktoré vnikajú do syncýtiotrofoblastu a tvoria základy budúcich choriových klkov - primárne choriové klky. Na 14. deň vývinu dovnútra primárnych klkov prenikajú bunky mezenchýmu z extraembryonálnej choriovej mezodermy, čím vznikajú sekundárne choriové klky. V 3. týždni vývinu do sekundárnych klkov prenikajú krvné kapiláry, čím vznikajú terciárne choriové klky. Terciárne choriové klky majú vaskularizované mezenchýmové vnútro, jednu vrstvu cytotrofoblastu (tzv. Langhansove bunky) a na povrchu vrstvu syncýtiotrofoblastu. Prítomnosť ciev v klkoch a v choriovej membráne umožňuje výmenu látok medzi krvou matky a plodovou krvou cez stenu klkov, čo predstavuje hemotrofný spôsob výživy. Krv matky preteká v medziklíkových priestoroch a obmýva povrch klkov.
Choriové klky vybíhají z choriové ploténky, jsou to prstovité výběžky placenty a umožňují maximální výměnu látek mezi matkou a plodem. Primární klky jsou vytvářené trofoblastem 13.-15. den vývoje zárodku. Jsou tvořené cytotrofoblastem a na povrchu pokryté vrstvou syncytiotrofoblastu. Sekundární klky vznikají 16.-21. den tak, že primární klky rostou směrem k decidua basalis. Terciální (placentové) klky vznikají 17.-22. den ze sekundárních, když se z buněk extraembryonálního mesodermu (který při vzniku primárních klků do nich vnikal) diferencují krevní buňky a vytvářejí krevní cévy, které tvoří kapilární sítě klků.
Štruktúra a funkcia placenty
Placenta sa skladá z fetálnej a materskej časti. Fetálna časť (pars fetalis placentae) vzniká z chorion frondosum a tvorí ju choriová platnička a choriové klky. Materská časť (pars materna placentae) pochádza z decidua basalis. Ľudská placenta je: hemochoriálna - materská krv priamo obmýva choriové klky. chorioallantois - podľa ciev, ktoré vaskularizujú choriovú časť. diskoidalis - má tvar kruhovitého alebo oválneho disku. olliformis (z gréckeho "olla" - hrniec) - pripomína hrniec, kde dno tvorí bazálna platnička deciduy, prikrývku choriová platnička a vnútro choriové klky.
Choriová platnička placenty je tvorená väzivom plodového obalu s vetvami pupočníkových ciev. Na strane obrátenej do amniálnej dutiny je pokrytá epitelom amnia. Placenta má priemer 15-20 cm, výšku 2-3 cm v strede a 4-6 mm na okraji. V termíne pôrodu váži 500-600 g, čo je približne jedna šestina hmotnosti plodu. Lidská placenta je hemochoriálna, čo znamená, že medzi materskou krvou a krvou plodu je bariéra tvorená plazmodiom, cytotrofoblastom, stromatom klkov a stenou kapilár. Táto bariéra sa počas tehotenstva postupne ztenčuje z 0,025 mm na 0,002 mm, čo uľahčuje prenos kyslíka a živín.
Základom placenty je choriálna platňa, do ktorej sa na plodovej ploche upína pupečník. Z pupečníka prechádzajú do platne dve pupočníkové artérie, ktoré sa v nej vetvia do kmeňov pre jednotlivé klky na maternální ploche placenty. Klky sa vetvia vajíčkovito a ich stromatom prechádzajú cievy až do kapilárnej siete na periferii klkov. V prvej polovici gestácie sú klky pokryté vrstvou syncýtiotrofoblastu a pod ňou vrstvou Langhansových buniek. Po 5. mesiaci sa syncýtiotrofoblast ztenčuje a Langhansove bunky takmer vymiznú. Koncom tehotenstva sa v stromate klkov zmenšuje väzivo a rozširujú sa cievy. Decidua basalis sa v druhom mesiaci gravidity rozvrství na povrchovú kompaktnú vrstvu a pod ňou uloženú vrstvu spongióznu. Z kompaktnej vrstvy vystupujú lištovité septá, ktoré vnikajú medzi okrsky klkov (kotyledony) a zabezpečujú zakotvenie placenty. Spongiózna vrstva má bohatú cievnu pleteň a jej stroma je redukované na tenké prepážky. Po pôrode sa placenta odplodí spolu s kompaktnou vrstvou decidua basalis práve v tejto spongióznej vrstve.
Funkcie placenty
Placenta plní viacero životne dôležitých funkcií:
- Látková výmena: Z materskej krvi do plodu prechádzajú živiny a kyslík. Plodové bunky využívajú tieto látky a vracajú späť matke odpadné produkty metabolizmu.
- Ochrana: Placenta vytvára imunitu pre plod na určitú dobu po narodení, najmä prostredníctvom prenosu imunoglobulínov IgG.
- Hormonálna produkcia: Placenta produkuje hormóny potrebné na udržanie tehotenstva, ako je progesterón. Začína produkovať progesterón koncom 3. mesiaca tehotenstva, čím umožňuje žltému teliesku zaniknúť.
Medziklíkové priestory placenty pojmú asi 150 ml krvi, ktorá sa každú minútu tri až štyrikrát vymení. Rozložená plocha klkov by dosiahla asi 10 metrov štvorcových, čo zabezpečuje maximálnu účinnosť výmeny.

Embryológia | Vývoj placenty
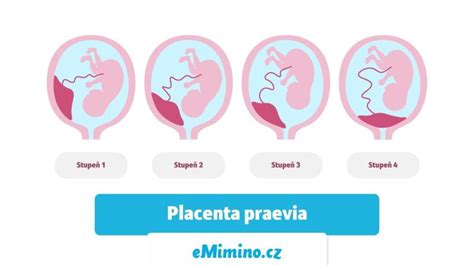
Anomálie placenty
Anomálie placenty môžu viesť ku komplikáciám počas tehotenstva a pôrodu. Placenta accreta complex je stav, pri ktorom sa placenta uchytí príliš hlboko do steny maternice. Predčasný odtok plodovej vody, dvoj- alebo viacpočetné tehotenstvo, poruchy zrážanlivosti krvi, predchádzajúca operácia maternice (napríklad cisársky rez), predchádzajúce problémy s placentou alebo užívanie návykových látok patria medzi rizikové faktory pre anomálie placenty.
Chorangióza
Chorangióza je vaskulárna zmena placenty s nejasnou etiológiou. Definovaná je nálezom minimálne 10 cievnych lúmenov v 10 klkoch v 10 neinfarktových plochách placenty hodnotených pri zväčšení objektívu 10x v 3 a viacerých kotyledónoch. Za fyziologických okolností obsahujú zrelé terminálne klky placenty zvyčajne 2 - 5 kapilár, ktoré sú dilatované a vypĺňajú časť klku. Vilózna hypervaskularita je charakterizovaná zvýšeným počtom cievnych priestorov, nesúvisiacich s ich dilatáciou ani venostázou.
V roku 1984 Altshuler definoval kritériá pre chorangiózu ako mnohopočetné kapilárne vaskulárne kľučky v koncových klkoch placenty s nálezom minimálne 10 cievnych lúmenov v 10 klkoch v 10 neinfarktových plochách placenty hodnotených pri zväčšení objektívu 10x v 3 a viacerých kotyledónoch. Incidencia chorangiózy stúpa so zvyšujúcim sa štádiom gravidity.
Etiologicky sa uvažuje najmä o význame hypoxie v etiológii chorangiózy. Toto tvrdenie by mohli podporovať poznatky o patofyziológii tvorby placentárnych ciev. Táto hypotéza však nebola nikdy jednoznačne potvrdená. V súlade s touto hypotézou je vyššia incidencia chorangiózy u žien žijúcich vo vyšších nadmorských polohách a u žien s ťažkými anemickými poruchami. Iné štúdie však signifikantnú spojitosť medzi hypoxiou a vznikom chorangiózy nenašli.
Chorangióza je často asociovaná s rôznymi fetálno-maternálnymi a placentárnymi zmenami, ako sú nálezy pupočníkových abnormalít vrátane prítomnosti len jednej umbilikálnej artérie aj vrodených vývojových chýb srdca plodu. Častejšie sa vyskytuje v súvislosti s preeklampsiou, hypertenziou alebo diabetom mellitom u matky, kde sa dáva do súvislosti so zmenami produkcie VEGF. Tieto stavy sú spojené so zvyšujúcou sa fetálnou a neonatálnou morbiditou aj mortalitou. Zdá sa však, že chorangióza tu predstavuje skôr vedľajší nález, ktorý vzniká ako následok choroby matky. Rizikovým faktorom je aj fajčenie.
Jedna z ďalších príčin vzniku chorangiózy môže byť aj hyperkapilarizácia spojená so vzostupom tlaku ako následok obštrukcie pupočníkovej žily. Možný je aj genetický alebo environmentálne získaný nesúlad medzi rastovými faktormi.
Problém v diferenciálnej diagnostike môže predstavovať venostáza placenty spojená s dilatáciou ciev bez zvýšenia ich počtu. Samotná ischémia tkaniva taktiež môže viesť k zmenám klkov v podobe ich „zošúverenia“ (shrinkage), ktoré sťažujú hodnotenie vaskularizácie a môžu viesť k jej nadhodnoteniu.
Imunohistochemické farbenie endotelových markerov CD31 a CD34 umožňuje lepšie a presnejšie hodnotenie počtu kapilár v porovnaní so štandardným farbením hematoxylínom a eozínom. Dôležité je aj odlíšenie chorangiózy od chorangiómu a chorangiomatózy.
Chorangiom predstavuje dobre ohraničené ložisko vyrastajúce z kmeňového klku, podobajúce sa kapilárnemu hemangiómu. V postihnutých klkoch dochádza k proliferácii kapilárnych štruktúr, prítomné sú endotelové bunky, pericyty aj myofibroblastové stromálne bunky. Cievne štruktúry pri chorangiomatóze majú hrubú stenu obsahujúcu hladkosvalové bunky pozitívne na aktín s podporným tkanivom tvoreným zvýšeným množstvom kolagénu, pričom nie sú viazané len na terminálne klky, ale obklopujú aj väčšie cievy v kmeňových klkoch. Kapiláry sú taktiež ohraničené kontinuálnou vrstvou pericytov pozitívnych na špecifický svalový aktín, na rozdiel od chorangiózy, kde pericyty netvoria kontinuálnu vrstvu okolo kapilár.
Opisuje sa, že chorangiom a fokálna alebo segmentálna chorangiomatóza sú častejšie prítomné v 32. - 36. týždni tehotnosti. Multifokálnu chorangiomatózu pozorujeme už v gestačnom veku nižšom ako 32. týždeň. Incidencia chorangiózy je nízka v 2. trimestri a stúpa v 3. trimestri, s maximom výskytu v neskorších štádiách tehotenstva.
Celková vaskularizácia klkov placenty stúpa so štádiom gravidity. Predpokladá sa, že chorangióza vyskytujúca sa bez nálezu iných príznakov hypoxie, fetálnej alebo maternálnej hypoperfúzie nepredstavuje riziko pre tehotnosť ani ju jednoznačne nemožno považovať za príčinu potratu alebo iných komplikácií tehotnosti. Naopak, rôzne choroby matky môžu zvyšovať pravdepodobnosť nálezu chorangiózy, ktorá by tak mohla predstavovať skôr faktor adaptácie placenty na zhoršené podmienky prostredia. Napriek všetkým teóriám ostáva príčina vzniku chorangiózy neznáma.
Opisujeme prípad 23-ročnej prvorodičky, u ktorej došlo v 25. týždni tehotnosti k abrupcii placenty s následným potratom mŕtveho plodu. Makroskopicky bola placenta prekrvácaná s retroplacentárnou krvnou zrazeninou, rozmerov 14 x 12 x 2,5 cm a hmotnosti 222 g. V mikroskopickom náleze sme pozorovali zväčšené klky s početnými cievami (10 a viac na jeden klk). Immunohistochemickým vyšetrením s použitím endotelového markera CD34 sme potvrdili zmnoženie malých cievnych lúmenov v jednotlivých klkoch.
Kmeňové bunky z placenty
V modernej medicíne sa kmeňové bunky využívajú na liečbu širokej škály chorôb. Iba počas pôrodu je možné získať a uchovať perinatálne tkanivá - pupočníkovú krv, tkanivo pupočníka a placenty. Sú to tie najmladšie zdroje kmeňových buniek s významným liečebným potenciálom. Keďže ide o bunky čerstvo narodeného dieťaťa, nie sú ovplyvnené ochoreniami získanými počas života či životným štýlom človeka.
„Pupočníková krv sa používa ako zdroj krvotvorných kmeňových buniek pri štandardnej liečbe - transplantácii krvotvorných kmeňových buniek, známejšej možno ako transplantácia kostnej drene,“ vysvetľuje molekulárna genetička MSc. Dominika Valent Raffajová. „Tá sa využíva napríklad pri onkologických a hematologických ochoreniach, ako sú leukémie, lymfómy, niektoré typy solídnych nádorov a anémie, ale aj na niektoré poruchy imunity či metabolické ochorenia.“
Prof. Dr. med. Wolfram C.M. Dempke bol počas svojej 30-ročnej kariéry v oblasti onkológii a hematológii pri množstve klinických štúdií. „Ukazuje sa, že kmeňové bunky odvodené z placenty môžu byť prospešné pri mnohých typoch ochorení, ako sú dysfunkcia vaječníkov, kardiovaskulárne ochorenia, ochorenia pečene, pľúc, obličiek, neurologické poruchy (mŕtvica, autizmus, skleróza multiplex), diabetes mellitus,“ potvrdzuje.
Doktor Nils Thoennissen, špecialista na internú medicínu, hematológiu a onkológiu z Mníchova, sa výskumom kmeňových buniek zaoberá už 15 rokov. „Za ten čas sa mi podarilo úspešne ich využiť v rôznych klinických podmienkach: pri liečbe pacientov, ktorí trpeli hematologickými ochoreniami, ako sú leukémia, myelóm a lymfóm, ale aj solídnymi nádormi, napríklad sarkómami,“ hovorí. Kmeňové bunky začal používať aj na regeneračné účely. Práve regeneratívna medicína je predmetom rozsiahleho výskumu, ktorý si okrem krvotvorných kmeňových buniek čoraz viac všíma aj tie mezenchymálne. „Viaceré štúdie mezenchymálnych kmeňových buniek pochádzajúcich z placenty preukázali porovnateľný, v mnohých prípadoch dokonca lepší terapeutický potenciál, aký vykazujú tieto bunky pochádzajúce z kostnej drene alebo z pupočnej šnúry,“ pokračuje Dr. med. Thoennissen. „Majú silnejšiu proliferačnú a regeneračnú schopnosť a čo je pozitívne, zároveň s minimálnym rizikom imunitnej reakcie.“ Výhodou je aj ich ľahká dostupnosť, neinvazívny postup pri ich získavaní a žiadne etické prekážky.
To, že tkanivo a bunky placenty dokážu znižovať zápal a regulovať imunitný systém, je dobre zdokumentované. Vďaka tejto skutočnosti sú predmetom záujmu tisícok štúdií na celom svete, ktoré skúmajú nové spôsoby liečby rôznych ochorení. Tkanivo placenty je najsľubnejším zdrojom buniek na použitie v bunkovej terapii.